
1.0철(Fe): 구조 재료의 기초이자 생명에 필수적인 원소

1.1물리적 및 화학적 특성:
- 금속 광택, 은회색 외관, 단단하지만 연성이 있음;
- 높은 융점(1539°C)으로 고온 가공에 적합합니다.
- 반응성이 있는 금속으로 산소, 물, 산과 쉽게 반응합니다.
- 일반적인 산화 상태는 +2와 +3입니다.
1.2주요 응용 분야:
제강:
철의 가장 중요한 용도는 강철 생산입니다. 강철은 철과 탄소의 합금으로, 강도, 인성 또는 내식성을 향상시키기 위해 종종 망간, 크롬, 니켈 및 기타 원소와 혼합됩니다. 강철은 다음과 같은 분야에서 널리 사용됩니다.
- 구조물 건설(예: 교량, 고층 건물)
- 기계 및 장비 제조
- 교통(자동차, 선박, 철도)
- 가전제품 및 생활용품


산업용 화학물질 및 비료:
철 화합물은 염료, 촉매, 수처리제 등을 생산하는 데 사용됩니다. 철분 기반 비료.
1.3생물학적 역할:
철은 생물에 필수적인 미량 원소입니다. 철의 주요 기능은 다음과 같습니다.
- 헤모글로빈과 미오글로빈을 구성하며 산소 운반에 관여함;
- 미토콘드리아 에너지 대사에 참여함;
- 다양한 효소와 단백질의 구성 요소로 사용됩니다.
1.4역사적, 문화적 중요성:
- 인간이 철을 이용하기 시작한 것은 철기 시대(기원전 1200년경)로 거슬러 올라가는데, 이때 철제 도구와 무기가 청동 도구를 대체하면서 농업 생산과 군사력이 크게 향상되었습니다.
- 철 제련 기술의 광범위한 도입은 인류 문명의 중요한 이정표가 되었습니다.
- 오늘날까지도 철은 전 세계적으로 가장 널리 사용되는 금속 재료입니다.
선택된 요소의 밀도
| 요소 | 밀도(g/cm3) | 모습 |
| 알류미늄 | 2.70 | 은백색, 금속성 |
| 안티몬 | 6.68 | 은백색, 금속성 |
| 카드뮴 | 8.64 | 은백색, 금속성 |
| 탄소(흑연) | 2.25 | 검은색, 둔한 |
| 크롬 | 7.2 | 스틸 그레이, 하드 |
| 코발트 | 8.9 | 은회색, 금속성 |
| 구리
금 |
8.92
19.3 |
붉은색, 금속성
노란색, 금속성 |
| 철 | 7.86 | 은, 금속 |
| 선두 | 11.3 | 은백색, 부드럽고 금속성 |
| 망간 | 7.2 | 회색 분홍색, 메탈릭 |
| 니켈
백금 |
8.9
21.4 |
은, 금속
은, 금속 |
| 규소 | 2.32 | 강철 회색, 결정질 |
| 은 | 10.5 | 은, 금속 |
| 주석(회색) | 5.75 | 회색 |
| 주석(흰색) | 7.28 | 흰색 금속 |
| 아연 | 7.14 | 청백색, 금속성 |
2.0밀도 이해: 정의, 계산 및 철의 예
2.1밀도란 무엇인가?
일반적인 밀도 단위는 다음과 같습니다.
- SI 단위: 킬로그램/세제곱미터(킬로그램/m³)
- 실험실 단위: 그램/세제곱센티미터(g/cm³) 또는 밀리리터당 그램(㎍/mL)
- 밀도는 일반적으로 그리스 문자로 표시됩니다. ρ(로)
2.2밀도 계산 공식
밀도(ρ) = 질량(m) / 부피(V)
어디:
- 질량은 일반적으로 다음과 같이 측정됩니다. 그램(g)
- 볼륨은 다음과 같이 표현될 수 있습니다. 밀리리터(mL)또는 입방 센티미터(cm³)
(참고: 1mL = 1cm³)
2.3예: 철 블록의 밀도
철 블록의 질량은 23.6그램, 치수는 다음과 같습니다. 2.0cm × 2.0cm × 0.75cm밀도를 확인하고 철로 만들어졌을 가능성이 있는지 확인하세요.
볼륨 = 2.0 × 2.0 × 0.75 = 3.0cm³
밀도 = 23.6g ÷ 3.0cm³ = 7.87g/cm³
결론:
물체의 밀도는 대략 다음과 같습니다. 7.87g/cm³이는 순수 철의 표준 밀도와 매우 유사합니다. 따라서 순수 철 또는 철 기반 합금일 가능성이 높습니다.
2.4철 및 철 합금의 밀도
밀도 순철 대략이다 7.874g/cm³
(또는 491.5 lb/ft³, 0.284 lb/in³)
아래 표는 실온에서 일반적인 철 및 철 합금의 밀도를 나타냅니다. 이 값은 재료 선택 및 공학 계산에 유용합니다.
| 철 및 철 합금의 밀도 | ||
| 재료 | 밀도 | |
| g/cm3 | 파운드중 / 안에3 | |
| 순철 | 7.874 | 0.2845 |
| 주괴 철 | 7.866 | 0.2842 |
| 단철 | 7.7 | 0.2 |
| 회주철 | 7.15 주-1 | 0.258 노트-1 |
| 가단성 철 | 7.27 주-2 | 0.262 노트-2 |
| 연성 주철 | 7.15 | 0.258 |
| 고니켈 철(Ni-Resist) | 7.5 | 0.271 |
| 고크롬 백철 | 7.4 | 0.267 |
참고-1: 6.95~7.35g/cm3(0.251~0.265lb/in.3).
참고-2: 7.20~7.34g/cm3(0.260~0.265lb/in.3).
3.0철의 밀도에 영향을 미치는 요인
3.1원자 구조
철의 밀도는 결정 구조에 영향을 받습니다.
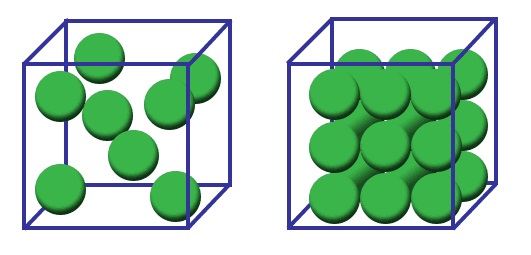
- 체심입방(BCC) 구조:페라이트(α-철, BCC)는 원자 패킹 효율성으로 인해 오스테나이트(γ-철, FCC)에 비해 밀도가 약간 낮습니다.
- 면심입방(FCC) 구조: 에서 발견됨 오스테나이트(γ-철), 을 가지고 있습니다 더 높은 밀도
3.2온도 및 상 전이
온도가 증가함에 따라 철은 결정 구조와 밀도에 영향을 미치는 상 전이를 겪습니다.
- α-철(BCC)로의 전환 γ-철(FCC) 대략 912°C
- γ-철(FCC)로 변형됩니다 δ-철(BCC) 약 1394°C
- 그만큼 녹는점철의 양은 대략 1538°
3.3합금 원소의 추가
- 다음과 같은 요소를 추가합니다. 탄소철의 구조와 밀도를 변화시킨다
- 예를 들어, 강철의 탄소 함량이 증가하면 다음과 같은 형성이 발생합니다. 펄라이트, 그리고 낮춥니다 상전이 온도주위에 727°C.
4.0철의 밀도에 대한 자주 묻는 질문
4.1순철의 밀도는 얼마입니까?
순수 철의 밀도는 실온에서 약 7.874g/cm³(또는 491.5lb/ft³, 0.2845lb/in³)입니다.
4.2철의 밀도는 온도에 따라 변합니까?
네, 철의 밀도는 결정 구조의 상전이로 인해 온도에 따라 달라집니다. 예를 들어, 912°C에서 α-철(BCC)은 밀도가 약간 더 높은 γ-철(FCC)로 변합니다.
4.3주철이나 연성 주철과 같은 철 합금의 밀도에 영향을 미치는 요소는 무엇입니까?
철 합금의 밀도는 합금 원소(예: 탄소, 니켈, 크롬)의 종류와 양, 그리고 미세 구조에 따라 달라집니다. 예를 들어, 회주철은 흑연 편상과 기공으로 인해 밀도가 더 낮습니다(약 7.15 g/cm³).
4.4철의 밀도는 어떻게 계산하나요?
밀도는 다음 공식을 사용하여 계산됩니다.
밀도(ρ) = 질량(m) / 부피(V)
예: 부피가 3.0cm³인 23.6g 철 블록의 밀도는 7.87g/cm³입니다.
4.5공학에서 철의 밀도가 중요한 이유는 무엇입니까?
철의 밀도는 재료의 무게, 구조 하중, 그리고 설계 타당성에 직접적인 영향을 미칩니다. 엔지니어들은 건물, 기계, 운송 수단의 재료를 선택할 때 밀도를 활용하여 강도, 무게, 그리고 비용의 균형을 맞춥니다.
다른: 알루미늄의 밀도
참고문헌:
https://www.princeton.edu/~maelabs/mae324/glos324/iron.htm
https://web.fscj.edu/Milczanowski/psc/lect/Ch4/slide6.htm
https://www.sciencedirect.com/topics/agricultural-and-biological-sciences/iron-fertilizers


