
1.0الحديد (Fe): أساس المواد الهيكلية وعنصر حيوي للحياة

1.1الخصائص الفيزيائية والكيميائية:
- بريق معدني، مظهر رمادي فضي، صلب ولكنه قابل للسحب؛
- نقطة انصهار عالية (1539 درجة مئوية)، مناسبة للمعالجة بدرجات حرارة عالية؛
- معدن نشط يتفاعل بسهولة مع الأكسجين والماء والأحماض؛
- حالات الأكسدة الشائعة هي +2 و +3.
1.2التطبيقات الرئيسية:
صناعة الصلب:
يُعدّ إنتاج الفولاذ أهم استخدامات الحديد. الفولاذ سبيكة من الحديد والكربون، تُخلط عادةً مع المنغنيز والكروم والنيكل وعناصر أخرى لتحسين القوة والمتانة ومقاومة التآكل. يُستخدم الفولاذ على نطاق واسع في:
- البناء الهيكلي (على سبيل المثال، الجسور والمباني الشاهقة)
- تصنيع الآلات والمعدات
- النقل (السيارات والسفن والسكك الحديدية)
- الأجهزة المنزلية والسلع اليومية


المواد الكيميائية والأسمدة الصناعية:
تُستخدم مركبات الحديد لإنتاج الأصباغ، والمحفزات، وعوامل معالجة المياه، الأسمدة التي تحتوي على الحديد.
1.3الدور البيولوجي:
الحديد عنصرٌ أساسيٌّ للكائنات الحية. وظائفه الأساسية تشمل:
- يشكل الهيموجلوبين والميوجلوبين، ويشارك في نقل الأكسجين؛
- المشاركة في عملية التمثيل الغذائي للطاقة الميتوكوندريا؛
- يدخل كمكون في تركيب العديد من الإنزيمات والبروتينات.
1.4الأهمية التاريخية والثقافية:
- يعود استخدام الإنسان للحديد إلى العصر الحديدي (حوالي 1200 قبل الميلاد)، عندما حلت الأدوات والأسلحة الحديدية محل الأدوات والأسلحة البرونزية، مما أدى إلى تقدم كبير في الإنتاج الزراعي والقدرات العسكرية؛
- لقد كان التبني الواسع النطاق لتكنولوجيا صهر الحديد بمثابة معلم رئيسي في الحضارة الإنسانية.
- وإلى يومنا هذا، يظل الحديد المادة المعدنية الأكثر استخدامًا على نطاق واسع في جميع أنحاء العالم.
كثافات العناصر المختارة
| عنصر | الكثافة (جم/سم3) | مظهر |
| الألومنيوم | 2.70 | أبيض فضي، معدني |
| الأنتيمون | 6.68 | أبيض فضي، معدني |
| الكادميوم | 8.64 | أبيض فضي، معدني |
| الكربون (الجرافيت) | 2.25 | أسود، باهت |
| الكروم | 7.2 | رمادي فولاذي، صلب |
| الكوبالت | 8.9 | رمادي فضي، معدني |
| نحاس
ذهب |
8.92
19.3 |
محمر، معدني
أصفر معدني |
| حديد | 7.86 | فضي معدني |
| يقود | 11.3 | أبيض فضي مزرق، ناعم، معدني |
| المنغنيز | 7.2 | رمادي وردي، معدني |
| النيكل
البلاتين |
8.9
21.4 |
فضي معدني
فضي معدني |
| السيليكون | 2.32 | رمادي فولاذي، بلوري |
| فضي | 10.5 | فضي معدني |
| القصدير (الرمادي) | 5.75 | رمادي |
| القصدير (الأبيض) | 7.28 | أبيض معدني |
| الزنك | 7.14 | أبيض مزرق، معدني |
2.0فهم الكثافة: التعريف والحساب والحديد كمثال
2.1ما هي الكثافة؟
تشمل وحدات الكثافة الشائعة ما يلي:
- وحدة النظام الدولي للوحدات:كيلوجرام لكل متر مكعب (كجم/م³)
- وحدات المختبر: جرام لكل سنتيمتر مكعب (جم/سم³) أو جرام لكل مليلتر (جم/مل)
- يتم تمثيل الكثافة عادة بالحرف اليوناني ρ (رو)
2.2صيغة حساب الكثافة
الكثافة (ρ) = الكتلة (م) / الحجم (فولت)
أين:
- يتم قياس الكتلة عادة بـ جرام (جم)
- يمكن التعبير عن الحجم بـ ملليلتر (مل)أو سنتيمتر مكعب (سم³)
(ملاحظة: 1 مل = 1 سم³)
2.3مثال: كثافة كتلة الحديد
كتلة الحديد لها كتلة قدرها 23.6 جرامًا، مع أبعاد 2.0 سم × 2.0 سم × 0.75 سم. تحديد كثافته وما إذا كان من المحتمل أن يكون مصنوعًا من الحديد.
الحجم = 2.0 × 2.0 × 0.75 = 3.0 سم³
الكثافة = 23.6 جم ÷ 3.0 سم³ = 7.87 جم/سم³
خاتمة:
الجسم له كثافة تبلغ حوالي 7.87 جم/سم³، وهي قريبة جدًا من الكثافة القياسية للحديد النقي. لذلك، يُرجَّح أن يكون حديدًا نقيًا أو سبيكة أساسها الحديد.
2.4كثافة الحديد وسبائك الحديد
كثافة الحديد النقي تقريبا 7.874 جم/سم³
(أو 491.5 رطل/قدم مكعب، 0.284 رطل/بوصة مكعبة)
يوضح الجدول أدناه كثافات أنواع الحديد الشائعة وسبائكه في درجة حرارة الغرفة. تُفيد هذه القيم في اختيار المواد والحسابات الهندسية.
| كثافة الحديد وسبائك الحديد | ||
| مادة | كثافة | |
| جم/سم3 | رطلم / في3 | |
| الحديد النقي | 7.874 | 0.2845 |
| سبائك الحديد | 7.866 | 0.2842 |
| الحديد المطاوع | 7.7 | 0.2 |
| الحديد الزهر الرمادي | 7.15 ملاحظة-1 | 0.258 ملاحظة-1 |
| الحديد القابل للطرق | 7.27 ملاحظة-2 | 0.262 ملاحظة-2 |
| الحديد المطاوع | 7.15 | 0.258 |
| حديد عالي النيكل (Ni-Resist) | 7.5 | 0.271 |
| الحديد الأبيض عالي الكروم | 7.4 | 0.267 |
ملاحظة 1: 6.95 إلى 7.35 جم/سم3 (0.251 إلى 0.265 رطل/بوصة3).
ملاحظة 2: 7.20 إلى 7.34 جم/سم3 (0.260 إلى 0.265 رطل/بوصة3).
3.0العوامل المؤثرة على كثافة الحديد
3.1البنية الذرية
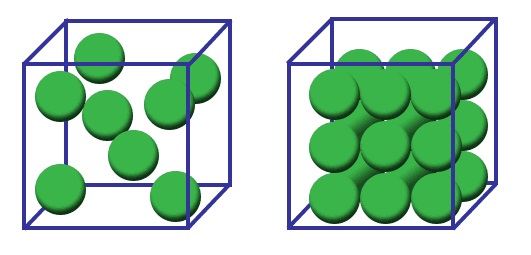
تتأثر كثافة الحديد ببنيته البلورية:
- هيكل مكعب مركزي الجسم (BCC):يتمتع الفريت (α-iron، BCC) بكثافة أقل قليلاً مقارنة بالأوستينيت (γ-iron، FCC) بسبب كفاءة التعبئة الذرية.
- هيكل مكعب مركزي الوجه (FCC):وجدت في أوستينيت (γ-حديد)، والتي لديها كثافة أعلى
3.2انتقالات درجة الحرارة والطور
مع ارتفاع درجة الحرارة، يخضع الحديد لتحولات طورية تؤثر على بنيته البلورية وبالتالي كثافته:
- الحديد ألفا (BCC)الانتقالات إلى الحديد جاما (FCC) في حوالي 912 درجة مئوية
- الحديد جاما (FCC)يتحول إلى حديد دلتا (BCC) في حوالي 1394 درجة مئوية
- ال نقطة الانصهارمن الحديد حوالي 1538 درجة
3.3إضافة عناصر السبائك
- إضافة عناصر مثل الكربونيغير بنية وكثافة الحديد
- على سبيل المثال، يؤدي زيادة محتوى الكربون في الفولاذ إلى تكوين بيرلايت، ويخفض درجة حرارة انتقال الطورإلى حول 727 درجة مئوية.
4.0الأسئلة الشائعة حول كثافة الحديد
4.1ما هي كثافة الحديد النقي؟
تبلغ كثافة الحديد النقي حوالي 7.874 جم/سم³ (أو 491.5 رطل/قدم³، 0.2845 رطل/بوصة³) في درجة حرارة الغرفة.
4.2هل تتغير كثافة الحديد مع درجة الحرارة؟
نعم، تختلف كثافة الحديد باختلاف درجة الحرارة نتيجةً لتحولات طور البنية البلورية. على سبيل المثال، عند درجة حرارة 912 درجة مئوية، يتحول الحديد ألفا (BCC) إلى الحديد غاما (FCC)، الذي يتميز بكثافة أعلى قليلاً.
4.3ما الذي يؤثر على كثافة سبائك الحديد مثل الحديد الزهر أو الحديد المطاوع؟
تعتمد كثافة سبائك الحديد على أنواع وكميات عناصر السبائك (مثل الكربون والنيكل والكروم) والبنية الدقيقة. على سبيل المثال، يتميز الحديد الزهر الرمادي بكثافة أقل (حوالي 7.15 جم/سم³) بسبب رقائق الجرافيت ومساميته.
4.4كيف يتم حساب كثافة الحديد؟
يتم حساب الكثافة باستخدام الصيغة:
الكثافة (ρ) = الكتلة (م) / الحجم (فولت)
مثال: كتلة حديدية تزن 23.6 جرامًا وحجمها 3.0 سم³ وكثافتها 7.87 جرامًا/سم³.
4.5لماذا تعتبر كثافة الحديد مهمة في الهندسة؟
تؤثر كثافة الحديد بشكل مباشر على وزن المادة، والحمل الهيكلي، وجدوى التصميم. يستخدم المهندسون الكثافة لاختيار مواد المباني والآلات ووسائل النقل لتحقيق التوازن بين القوة والوزن والتكلفة.
آخر: كثافة الألومنيوم
مراجع:
https://www.princeton.edu/~maelabs/mae324/glos324/iron.htm
https://web.fscj.edu/Milczanowski/psc/lect/Ch4/slide6.htm
https://www.sciencedirect.com/topics/agricultural-and-biological-sciences/iron-fertilizers


